Biomaterials:铜驱动的双重细胞死亡可破坏细胞内氧化还原稳态以实现抗肿瘤免疫治疗
奇物论
2025-07-20 21:52
文章摘要
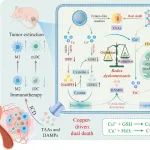
本文介绍了一种铜基纳米诱导剂(CST NPs),用于通过破坏细胞内铜离子稳态同时诱导铜死亡和双硫死亡,以实现抗肿瘤免疫治疗。研究背景指出,肿瘤内氧化还原稳态的异常是促进肿瘤生长和转移的重要因素。研究目的是开发一种能够精准调节细胞内还原机制的铜基纳米诱导剂。实验结果表明,CST NPs在酸性肿瘤微环境中能够抑制G6PD活性,减少NADPH的产生,并显著消耗GSH合成所需的底物,从而破坏细胞氧化还原稳态。此外,CST NPs还能诱导细胞骨架收缩和破裂,释放肿瘤相关抗原和损伤相关分子模式,重编程免疫抑制TME以启动有效的免疫应答。结论是该研究为铜诱导细胞死亡的机制提供了新的理论基础。
本站注明稿件来源为其他媒体的文/图等稿件均为转载稿,本站转载出于非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性。如转载稿涉及版权等问题,请作者速来电或来函联系。